2024年11月14日,禾沐基因研发团队在《Clinical and Translational Medicine》(中科院一区)上发表了题为“Molecular characterization of human HSPCs with different cell fates in vivo using single-cell transcriptome analysis and lentiviral barcoding technology”的研究论文。研发团队将
单细胞转录组测序技术与慢病毒条形码技术结合创造了SCALeBa(Single-Cell transcriptome Analysis and Lentiviral Barcoding)技术,用于研究体内人类造血干细胞&祖细胞(HSPCs)在不同细胞命运下的分子特征。
通过使用 SCALeBa 技术结合小鼠体内移植实验,将HSPCs根据其干性和分化偏好性划分为若干亚群,通过鉴定不同HSPCs亚群的分子特征,基因层面对人类造血干细胞异质性进行解释。
 人类造血干细胞&祖细胞(HSPCs)是造血系统的基础,它们负责长期维持和持续产生所有成熟的血细胞谱系,在整个生命周期中都发挥着至关重要的作用。同时,基于 HSPCs 的异体干细胞移植在临床上已广泛应用于治疗各种血液恶性肿瘤和遗传性血液疾病,包括依赖输血的β地中海贫血和先天性免疫缺陷。因此,深入了解 HSPCs 的异质性及其维持干性和分化偏好的分子机制对基础科学研究和临床应用都非常重要。本研究提出了一种将单细胞转录组技术与慢病毒条形码技术结合的SCALeBa(Single-Cell transcriptome Analysis and Lentiviral Barcoding)技术,用于研究体内HSPCs异质性的分子机制。SCALeBa技术可以在追踪单个细胞分化命运的同时获取其单细胞转录组基因表达谱等信息,将谱系示踪的分辨率提高到了单细胞级别。研究结果表明,具有较强干性的 HSPC 亚群高表达 MYL6B、ATP2A2、MYO19、MDN1、ING3 等基因。而COA3、RIF1、RAB14、GOLGA4等基因的高表达可能有助于HSPC向着多谱系分化。此外,本研究通过生物学实验以及公共数据集证实了上述基因对于HPSCs干性以及分化偏好性的作用。同时,研究表明,高表达MRPL23和RBM4 基因的 HSPCs 可能分别倾向于分化为髓系和淋系细胞类群。最后,研究证实,使用SCALeBa进行单细胞层面的谱系示踪提高了Monocle2拟时序分析结果的准确性。综上所述,SCALeBa技术为解析体内HSPCs的异质性提供了新的见解,为干细胞研究领域提供了新的工具。
人类造血干细胞&祖细胞(HSPCs)是造血系统的基础,它们负责长期维持和持续产生所有成熟的血细胞谱系,在整个生命周期中都发挥着至关重要的作用。同时,基于 HSPCs 的异体干细胞移植在临床上已广泛应用于治疗各种血液恶性肿瘤和遗传性血液疾病,包括依赖输血的β地中海贫血和先天性免疫缺陷。因此,深入了解 HSPCs 的异质性及其维持干性和分化偏好的分子机制对基础科学研究和临床应用都非常重要。本研究提出了一种将单细胞转录组技术与慢病毒条形码技术结合的SCALeBa(Single-Cell transcriptome Analysis and Lentiviral Barcoding)技术,用于研究体内HSPCs异质性的分子机制。SCALeBa技术可以在追踪单个细胞分化命运的同时获取其单细胞转录组基因表达谱等信息,将谱系示踪的分辨率提高到了单细胞级别。研究结果表明,具有较强干性的 HSPC 亚群高表达 MYL6B、ATP2A2、MYO19、MDN1、ING3 等基因。而COA3、RIF1、RAB14、GOLGA4等基因的高表达可能有助于HSPC向着多谱系分化。此外,本研究通过生物学实验以及公共数据集证实了上述基因对于HPSCs干性以及分化偏好性的作用。同时,研究表明,高表达MRPL23和RBM4 基因的 HSPCs 可能分别倾向于分化为髓系和淋系细胞类群。最后,研究证实,使用SCALeBa进行单细胞层面的谱系示踪提高了Monocle2拟时序分析结果的准确性。综上所述,SCALeBa技术为解析体内HSPCs的异质性提供了新的见解,为干细胞研究领域提供了新的工具。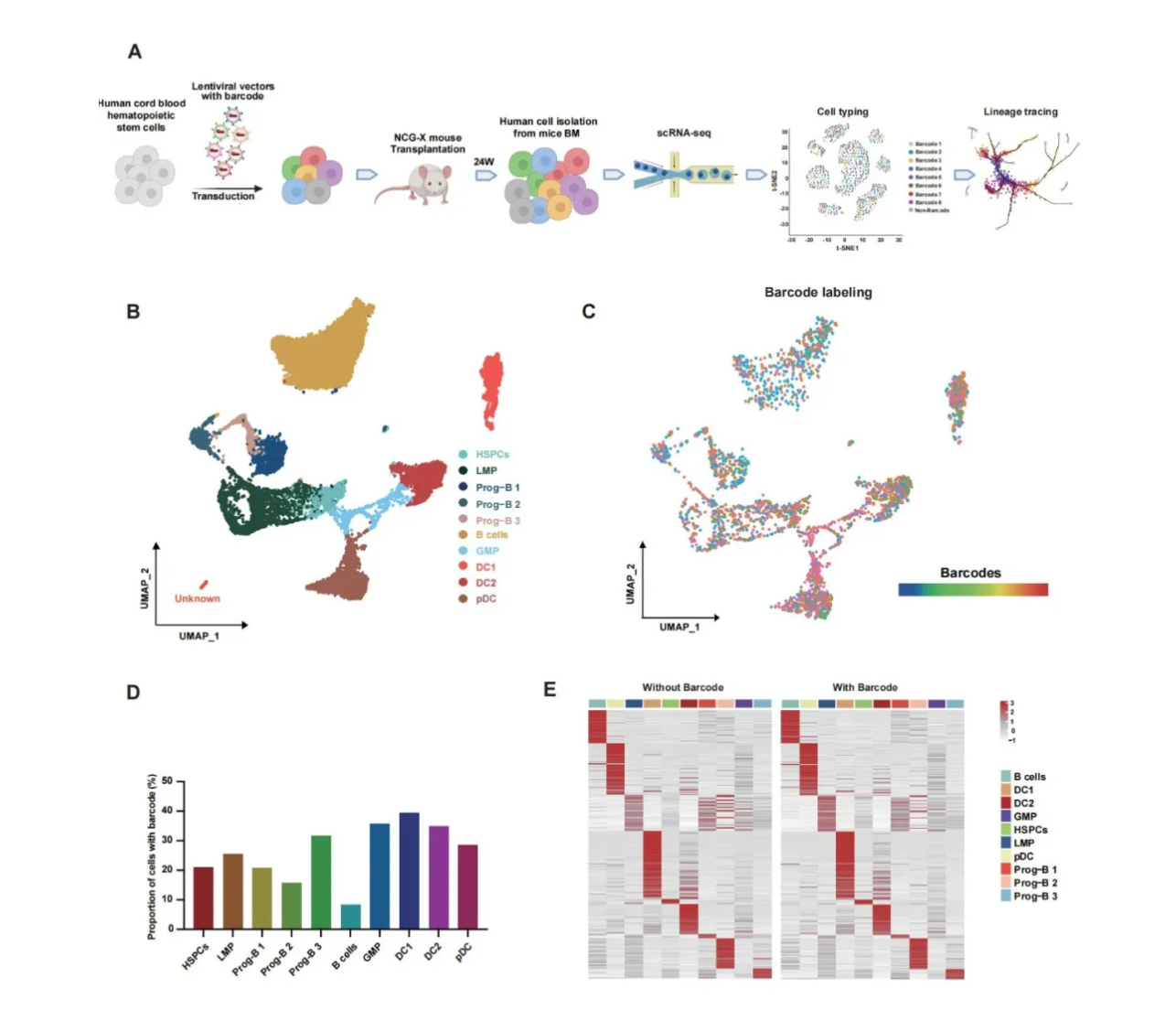
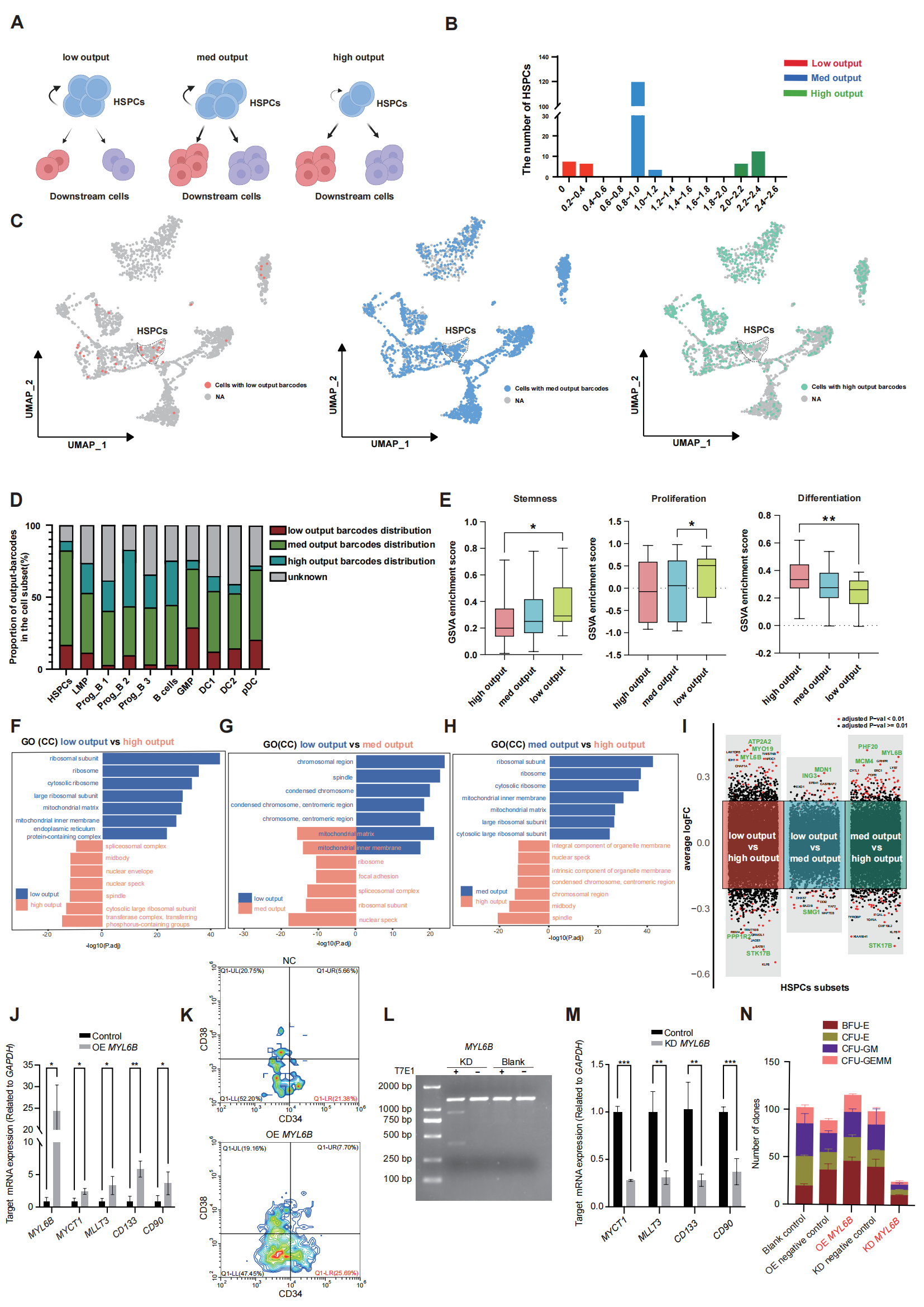 谱系示踪探索人造血干细胞体内维持干性关键因素
谱系示踪探索人造血干细胞体内维持干性关键因素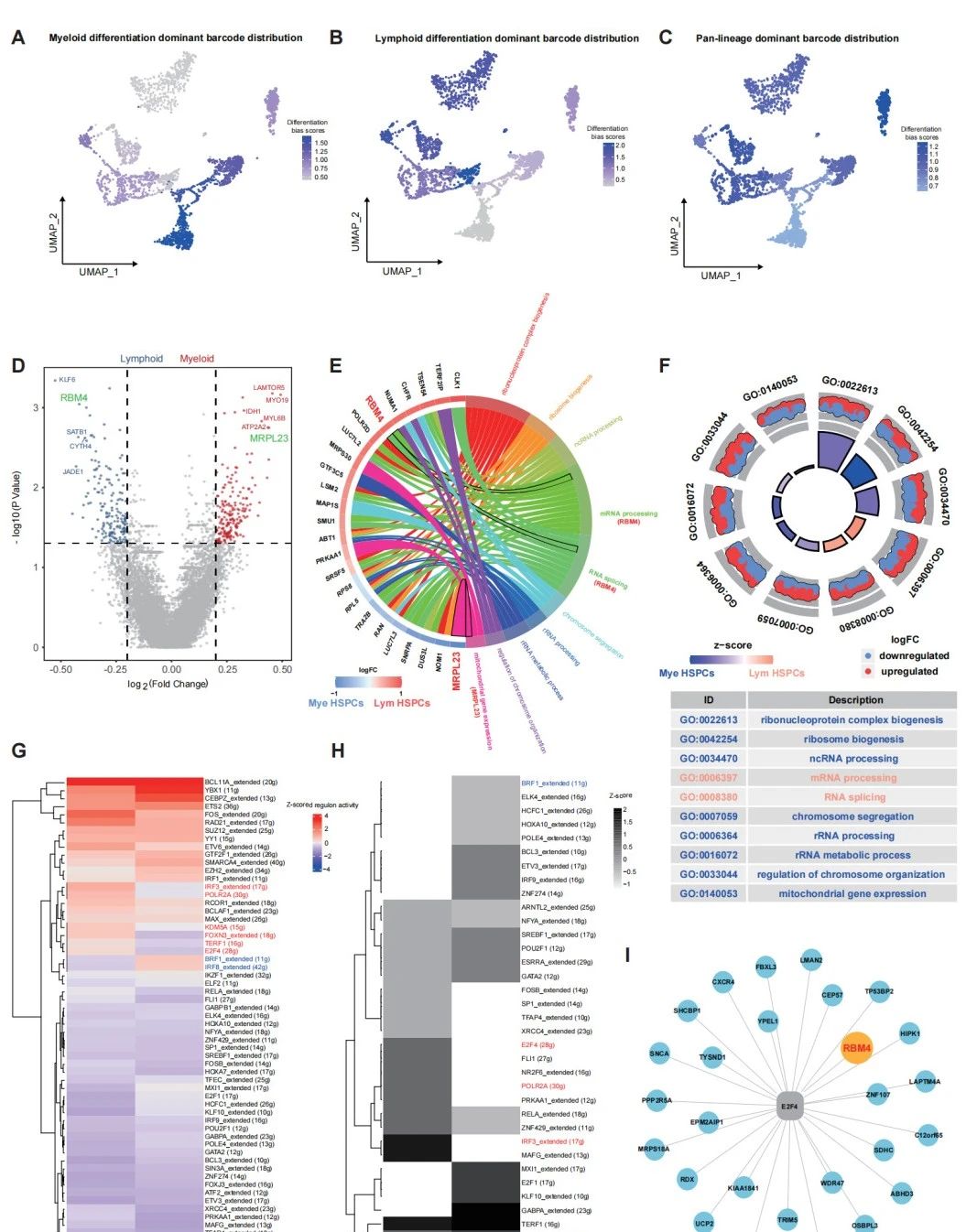 谱系示踪探索人造血干细胞体内分化偏好性关键因素
谱系示踪探索人造血干细胞体内分化偏好性关键因素
SCALeBa技术平台的原理是利用了慢病毒载体携带外源基因片段插入受体细胞基因组中并长期稳定表达的特点,将20bp的标签序列插入受体细胞基因组中。对受体细胞进行单细胞测序后,利用生信分析手段对细胞中的标签序列进行提取与分析以达到谱系示踪的目的。相较于传统的谱系示踪手段,该技术在了解单个细胞的基因表达特征的同时,利用标签序列更加准确的描绘了细胞的分化轨迹。通过检测下游细胞的标签序列的组成和分布,可以获得有关上游细胞的异质性、发育和分化轨迹,分化偏好等信息(见下图SCALeBa技术路线)。干细胞、免疫学、发育生物学、血液类疾病研究等领域,获取单个细胞的基因表达特征的同时,揭示细胞异质性,细胞发育和分化过程,探索细胞的功能等。可用于体外培养细胞,体内移植等。
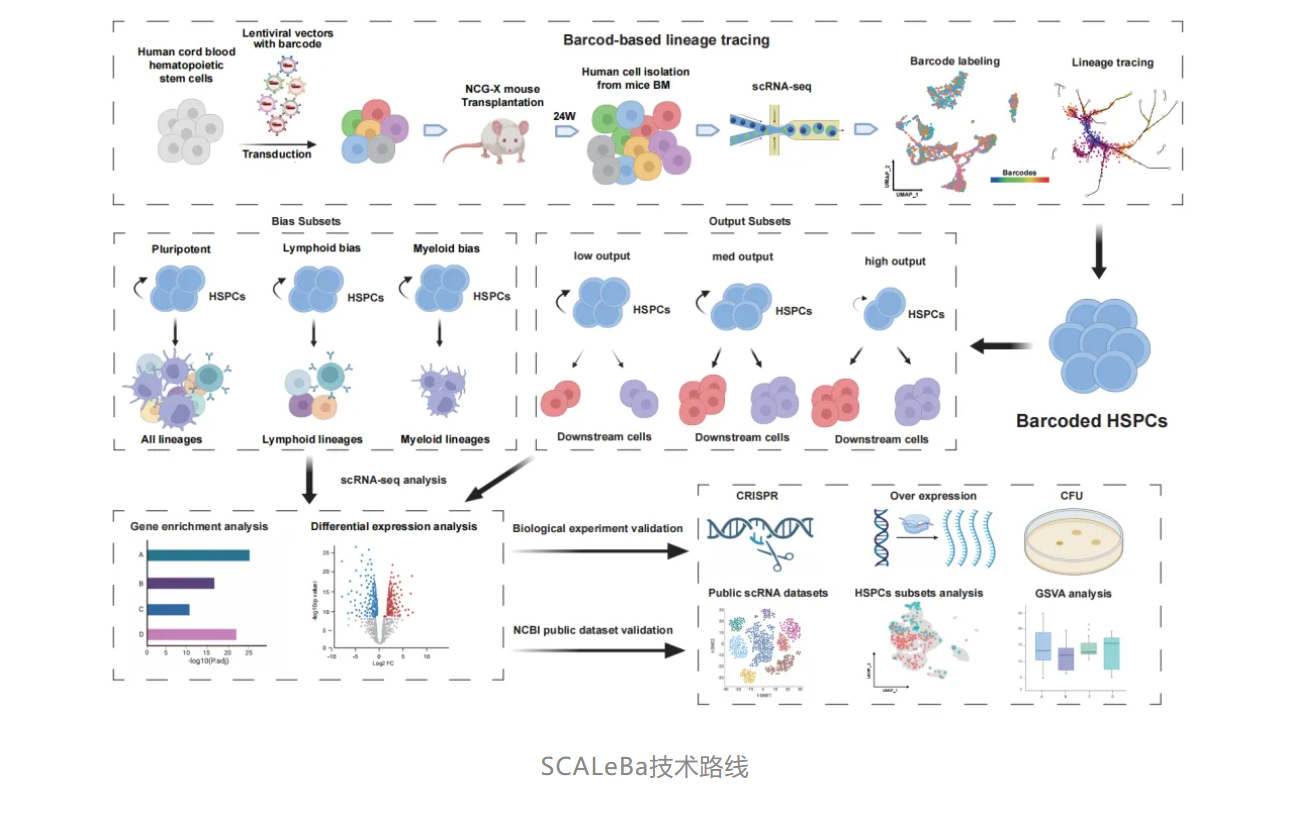
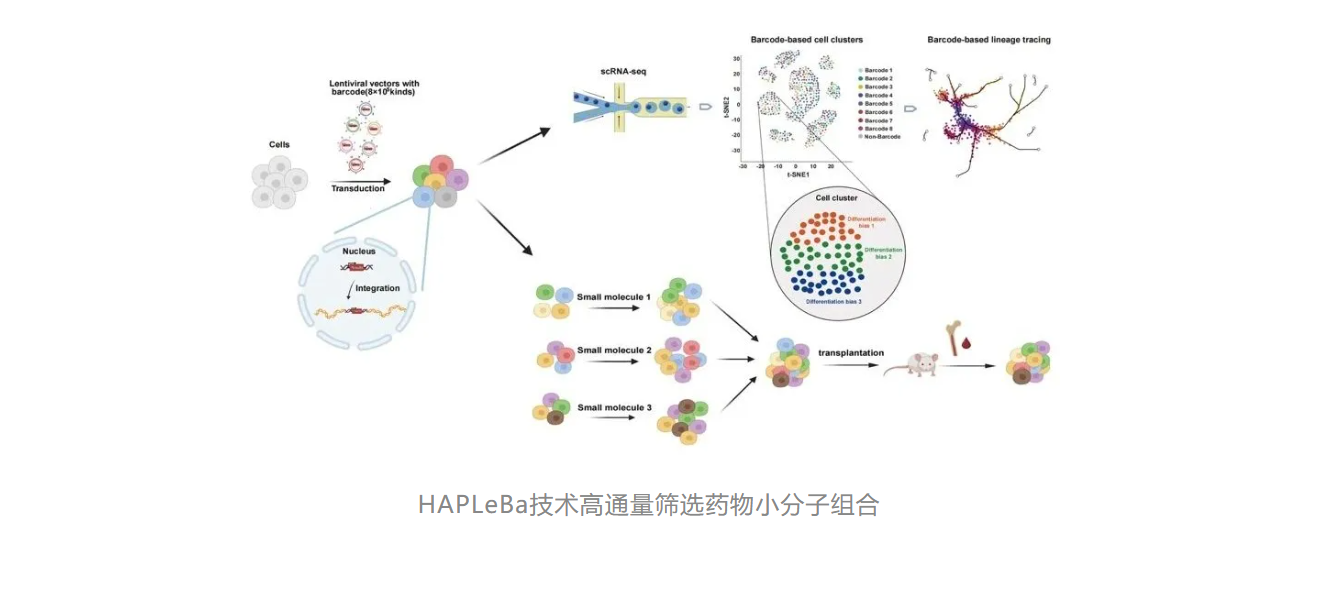
慢病毒标签高通量分析平台-HAPLeBa (High-throughput Analysis Platform Based on Lentiviral Barcoding)原理同样是利用了慢病毒载体携带外源基因片段插入受体细胞基因组中并长期稳定表达的特点,将20bp的标签序列插入受体细胞基因组中。对受体细胞基因组或转录组进行二代测序及其他高通量测序后,利用生信分析手段对细胞中的标签序列进行提取与分析以达到谱系示踪的目的。可用于体外培养细胞,体内移植,高通量药物小分子筛选、药品生产工艺优化等。
1. 先进的平台:国内顶尖的 MGI-DNBelab C系列单细胞测序技术平台、BGI高通量测序平台。2. 强大的技术实力和经验:成熟慢病毒、基因编辑技术产线,丰富的慢病毒改造、转导经验。
3. 成熟的数据分析能力:依托华大基因顶尖的生物信息平台以及优秀的生物信息分析团队,能够提供全面的数据分析服务以及结果解读。2. 基础服务:提供标签慢病毒文库以及后续的标签抓取、分析服务;3. 高阶定制:提供慢病毒文库转染以及单细胞/其他高通量建库测序、数据下机后的标签抓取、示踪分析等服务。


 谱系示踪探索人造血干细胞体内维持干性关键因素
谱系示踪探索人造血干细胞体内维持干性关键因素 谱系示踪探索人造血干细胞体内分化偏好性关键因素
谱系示踪探索人造血干细胞体内分化偏好性关键因素



 谱系示踪探索人造血干细胞体内维持干性关键因素
谱系示踪探索人造血干细胞体内维持干性关键因素 谱系示踪探索人造血干细胞体内分化偏好性关键因素
谱系示踪探索人造血干细胞体内分化偏好性关键因素
